Polimeraz Zincir Reaksiyonu (PCR) Yöntemi ve Real-Time PCR
PCR Tarihçesi;
1985’de bilim dünyasına sunulduğundan itibaren polimeraz zincir reaksiyonu (PCR); hem araştırmada hem de klinik laboratuvarlarda tanıda yeni bir çığır açmıştır. ABD’de Henry A. Erlich, Kary Mullis ve Randall K. Saiki tarafından geliştirilmiştir.

PCR’ın Temel Prensipleri;
Polimeraz zincir reaksiyonu (PCR), in vitro koşullarında DNA dizilerinin çoğaltılması esasına dayanmaktadır.
PCR; Basit, spesifik ve hassas bir tekniktir.
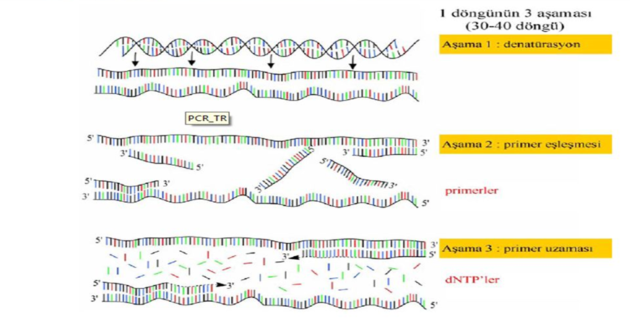
Üç basamaktan (denaturation, annealing, primer extension) oluşan işlem, bir PCR devrini temsil eder.
Bu işlem, genel olarak 25 ile 40 defa tekrar edilerek başlangıçtaki DNA dizisinden milyonlarca yeni DNA parçacığı çoğaltılır.
PCR sonucunda elde edilen DNA parçacıkları agaroz veya poliakrilamit jellerde yürütüldükten sonra, ethidium bromide (EtBr) veya gümüş nitrat (GN) ile boyanarak gözlemlenir.
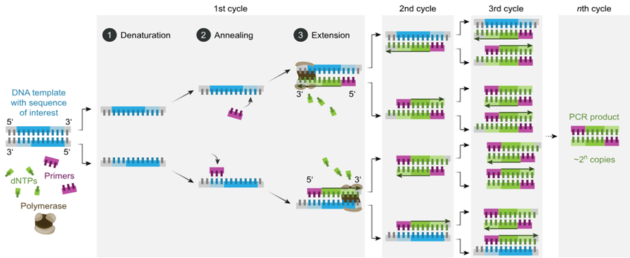
1) DNA Zincirinin Açılması (Denaturation);
Kalıp DNA (template DNA), 92-95 derecede 1-2 dakika tutularak çift sarmal yapıdaki DNA iplikçikleri birbirlerinden ayrılmaktadır. DNA zincirini ayırmak için, bazı durumlarda 5-10 dakika ön ısıtma yapmak gerekebilir.
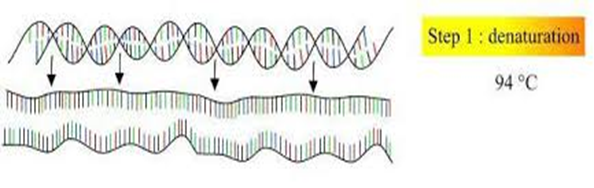
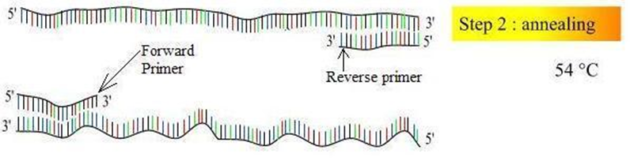
2) Primerlerin Açılan DNA Zincirlerine Yapışması (Annealing);
Reaksiyon sıcaklığının, 37-65 dereceye düşürülerek oligonükleotid primerlerinin açılan DNA zincirlerinin kendi baz dizilerine karşılık gelen bölgeye yapışması işlemidir. Bu işlem, üretilecek baz uzunluğuna bağlı olarak saniyede gerçekleşmektedir.
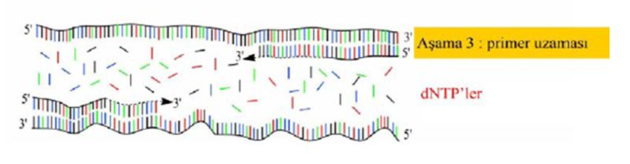
3) Primer Uzaması (Primer Extesion);
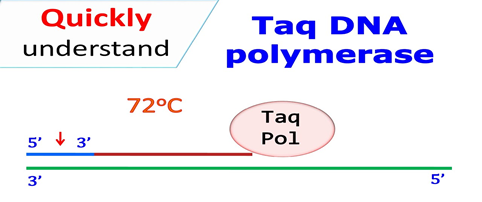
DNA zincirleri üzerine yapışan primerlerin DNA polimeraz enzimi (Taq DNA polymerase) vasıtasıyla uzatılmasıdır. Taq DNA polymerase 72 derece sıcaklıkta daha iyi çalıştığı için genel olarak tüm çoğaltma işlemleri bu sıcaklıkta yapılmaktadır.
PCR Çalışmalarında Kullanılan Malzemeler;
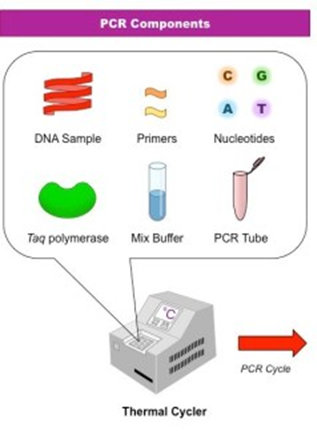
Distile su
Buffer (tampon çözeltisi-1XTBE)
MgCl2
Dinükleotittrifosfatlar (dNTP)
Primerler (forward ve revers)
Taq DNA polimeraz
Çoğaltılmak istenen DNA (kalıp-template DNA)
Kalıp DNA;
Çoğaltılacak bölgeye üzerinde taşıyan DNA’dır. Bu bölge için kalıp olma görevi vardır. PCR’de; genomik DNA’lar, plazmid ve faj DNA’ları çeşitli genler ve hatta herhangi bir DNA parçası kalıp olarak kullanılabilir. PCR’de kalıp olarak DNA’nın yanı sıra RNA’da kullanılabilir. Bu kalıp DNA’lar amaca göre cDNA, genomik DNA, genom kitaplıkları şeklinde ya araştırma laboratuarları yada kliniklerden ticari olarak temin edilebilir.
Dna Polimerazlar;
Bu enzimler kalıp DNA’ya bağlanmayı kolaylaştırıp, yeni bir iplik oluşturmak üzere uzun polipeptidten zincirin sentezini kataliz eder.
Sentezi başlatmak için primerlere ihtiyaç duyarlar. 5 ’ uçtan 3 ’ uca doğru, primerin serbest 3 ’ hidroksil ucuna ortamdaki dNTP’lerin nükleofilik etki yapmalarıyla, fosfodiester bağlarının katalizi ve yeni DNA ipliğinin polimerizasyonu sağlanmış olur.
Primerler;
Reaksiyonun özgülüğü primer oligonükleotidlerin seçilmesiyle sağlanır. Bunlar amplifiye edilecek DNA’ ya bağlanacak olan bağlanma bölgesine komplementer yapıda kısa tek sarmal DNA molekülleridir. Primerler çiftler halinde biri çift zincir DNA’yı oluşturan zincirlerinden birine, diğeri de o zincirin komplementerine eşleşecek şekilde farklı dizilimlerde tasarlanırlar. Amplifikasyon için DNA dizisinin bilinmesi gerekli değildir. Birleşme bölgelerinin dizisinin bilinmesi yeterlidir.
dNTP Karışımı;
Deoksirübonükleozid trifosfatlar, (dATP,dGTP,dTTP,dCTP), yüksek saflıkta ya tek tek ya da dörtlü karışım halinde ticari olarak bulunur. DNA sentezi için gereklidir.
Tamponlar ve Magnezyum;
Tamponlar, enzim için gerekli olan elektrolitleri ve koenzimleri sağlar. Yine polimeraz enzimleri aktiviteler için serbest magnezyum iyonlarına gereksinim duyarlar. Bu yüzden magnezyum içeren tamponlar kullanılır. Tampon çözeltisinin içeriği kullanılan enzimin tipi ve özelliğine göre seçilir. PCR’de en çok kullanılan tampon Taq/Amplitaq enzimlerine özgü olan tampondur.
Mg+2 iyonları;
1. dNTP’ler ile çözünebilir kompleksler oluştururlar.
2. Polimeraz aktivitesini arttırır.
3. Çift iplikli DNA’nın Tm (erime noktasını) değerini arttırırlar.
4. Primer/kalıp etkileşimini sağlarlar.
Pcr Aşamaları;
Başlangıçtaki DNA molekülü sayısı PCR’ ın kaç döngü uygulanacağını belirler. 1- 100 kopya DNA molekülü ile başlanıyorsa 20-30 döngü, 1.000 – 100.000 ile başlanıyorsa 30-45 döngü yeterlidir.
Bir döngü sonucunda başlangıçta n olan DNA zincir sayısı 2n’ e yükselir. Döngüler arka arkaya çok kez tekrarlanırken her bir döngünün ürünü, bir sonrakinde kalıp olarak kullanıldığı için her döngüde istenen DNA fragmenti miktarı 2 katına çıkar.
PCR’a başlamadan önce primer dizaynı yapılmalıdır. İstenen bölgenin çoğaltılması için o bölgeye özgü primerler yapılır. Primer boyutu 18-22 baz çifti arasındadır. Daha düşük sayıda primer üretilirse primerin özgüllüğü azalır, yükseltilirse de primerin bağlanması kalıp DNA’ya bağlanması güçleşir.
Primerlerin annealing derecelerinin hesaplanması: 2 (A+T)+4 (G+C)
Örnek dizi: 5’-ccttaagctggtgtccaaat-3’ 2(11AT)+4(9GC)=58ºC 5’-gctagcaatatttgtaagcat-3’, 2(14AT)+4(7GC)=56 ºC
PCR Optimizasyonu;
PCR şartları yeni PCR uygulaması için uygun bir şekilde yeniden ayarlanmazsa bazı problemlerle karşılaşılabilmektedir.
Bu problemler;
- PCR’dan beklenen ürün ya az alınır ya da hiç alınmaz.
- Primerlerin yanlış bağlanmasından dolayı spesifik olmayan bantlar oluşabilir.
- Primerler yanlış şekilde uzayabilir.
- Primer-dimer oluşumu ortaya çıkabilir ve bu oluşumlar çoğaltma işlemini yavaşlatır.
- Yeni sentezlenen DNA dizilerinde mutasyon veya istenilenden farklı diziler ortaya çıkabilir.
PCR Çalışma Şartlarını Etkileyen Faktörler;
1- Enzim Konsantrasyonu;
Diğer PCR şartları optimum seviyede olduğu zaman 100 μl reaksiyon için önerilen Taq DNA polimeraz enzim konsantrasyonu ünitedir.
Fakat enzim gereksinimi kullanılan kalıp DNA veya primere göre değişebilir.
Enzim konsantrasyonu düşük olursa elde edilecek ürün (DNA) az olur.
Enzim konsantrasyonu yüksek olursa spesifik olmayan bantlar ortaya çıkabilir.
2- Magnezyum Konsantrasyonu;
Mg konsantrasyonu primerlerin açılan DNA zincirlerine yapışmasını, kalıp DNA’nın açılma sıcaklığını, PCR sonucunda elde edilen DNA kalitesini, primer-dimer bağ oluşumlarını, enzim aktivitesi ve güvenilirliğini etkilemektedir.
Taq DNA polimeraz enziminin iyi bir şekilde çalışabilmesi için; kalıp DNA, primerler ve nükleotid bazları üzerinde serbest Mg iyonlarının bulunması gerekir.
3- Deoksinükleotid Trifosfatlar (Deoxynucleotide Triphosphates=dNTPs);
dNTP konsantrasyonunun yüksek olması yeni sentezlenen DNA dizilerinde istenilenden farklı dizilerin (misincorporation) hatalı olarak ortaya çıkmasına sebep olabilir.
Bu yüzden mümkün olduğu kadar düşük konsantrasyonda dNTP’leri kullanmak PCR spesifikliğini ve güvenilirliğini artırmaktadır.
4) DNA Zincirinin Açılması İçin Gerekli Zaman ve Sıcaklık;
PCR uygulamalarında sistemin çalışmamasının en önemli sebeplerinden birisi kalıp DNA zincirinin veya üretilen DNA parçacığının yeterince açılmamasıdır.
Genel olarak DNA moleküllerinin 95 oC de 2 dakika tutulması zincirin açılması için yeterli olmaktadır. Fakat GC bazlarınca zengin kalıp DNA zincirlerinde bu süre ve sıcaklığın fazla olması istenmektedir.
5- Primerlerin Açılan DNA Zincirlerine Yapışması;
Primerlerin açılan DNA zincirlerine yapışması için gerekli sıcaklık derecesi ve zaman aralığı primerlerin konsantrasyonu, elde edilecek DNA’nın uzunluğu ve kullanılan bazların kompozisyonuna göre değişir.
Primerler açılan DNA’ya bağlanması sırasında sıcaklığın artırılması DNA seçiciliğini artırmaktadır.
Dolayısıyla primerlerin yanlış yerlere bağlanması ve hatalı DNA dizilerinin elde edilmesi önlenmiş olmaktadır.
Özellikle PCR işleminin ilk birkaç devrinde sıcaklığın artırılması PCR uygulamasının hassasiyetini çok yükseltmekte ve spesifik olarak beklenen DNA parçacıkları sentezlenmektedir.
Sıcaklığın düşürülmesi primerlerin hatalı şekilde uzamasına ve yeni sentezlenen DNA dizilerinde hatalı baz bağlanmalarına sebep olmaktadır.
6- Primer Uzunluğu;
Konsantrasyonu ve Yapısı Yüksek primer konsantrasyonu primerlerin yanlış bağlanmasına ve spesifik olmayan DNA bantlarının üretilmesine sebep olur. Ayrıca primer-dimer oluşumunu teşvik ederek elde edilecek ürünün (DNA) az olmasına sebep olmaktadır.
Primerlerin yapışma sıcaklığını hesaplamak için bir formül geliştirilmiştir. Bu formül Tm= 4 (G+C) + 2 (A+T) şeklinde ifade edilmiştir. Burada Tm yapışma sıcaklığını, G,C,A ve T ise nükleotid bazlarını ifade etmektedir.
7- Devir Sayısı;
PCR’ın çalışma şartları iyi ayarlandığı taktirde devir sayısı yeterli olmaktadır.
Devir sayısının fazla olması spesifik olmayan bantların ortaya çıkmasına, devir sayısının az olması üretilen DNA miktarının az olmasına sebep olmaktadır.
PCR Kullanım Alanları;
Kalıtsal hastalıklarda taşıyıcının ve hastanın tanısında
Klinik örneklerde patojen organizmaların saptanmasında
Adli tıptaonkogenesisin araştırılmasında
Klonlamada / gen ekspresyon araştırmalarında
DNA dizi analizinde, büyük miktarda DNA örneklerinin oluşturulmasında
Bilinmeyen dizilerin belirlenmesinde
Geçmiş DNA’nin incelenmesi ve evrimin aydınlanmasında
Restriksiyon Fragment Length Polimorfizm (RFLP) Analizinde
Gen aktarılmış bitkilerin ve DNA baz dizilerinin belirlenmesi
Real Time PCR;
Son yılllarda PCR reaksiyonlarında sıcaklık döngüleri sağlamak için kullanılan cihazların (thermocycler) hassas ölçüm aletleriyle birleştirilmesi, real-time PCR olarak adlandırılan yeni bir yöntemin gelişmesine neden olmuştur.
Real-time PCR’da ürünlerin analizi reaksiyon sırasında yapılmaktadır.
Bu nedenle, agaroz jel elektroforezi, DNA bantlarının mor ötesi ışık altında görüntülenmesi gibi işlemlerin uygulanmasına gerek kalmamaktadır.
Real-time PCR ürünlerinin kalitatif ve kantitatif analizlerinde, diziye özgün olmayan floresan boyalardan ya da diziye özgün problardan yararlanılmaktadır.
Klasik PCR’da Problemler;
- Primer seçimi ve dizaynı
- Termalcycler programları
- Reaksiyon şartları
- Zaman alan analiz işlemleri
- Bir testin optimizasyonu
- Agaroz jel elektroforezi
- Blotlama
- Kontaminasyon riski
Real-Time PCR’ın Avantajları;
- Spesifik olmayan amplifikasyonlardan etkilenmiyor
- Reaksiyon boyunca veri toplanarak aynı anda analiz imkanı
- PCR sonrası ürünlerin ikincil bir işlemi gerekmiyor(yüksek verimlilik,düşük kontaminasyon riski)ultra-rapid siklus (30 dak. to 2 saat)10¹º katı bulan geniş dinamik aralık
- İki kat değişikliği hızla tanımlayabilmekte
- Spesifik erime eğrisi analizleri ile spesifikamplifikasyonların tanımlanması
- Duyarlılığı, özgüllüğü ve tekrarlanabilirliği yüksek
- Konvensiyonel PCR’dan daha pahalı değildir.
Real-Time PCR’ın Dezavantajları;
- Teknik donanım, alt yapı, beceri ve tecrübe gerektiriyor
- Yüksek ekipman ihtiyacı
- Aynı ve farklı laboratuvar’lar arasında sonuçlar arası faklılıklar
- Standardizasyon problemi
Kaynaklar;
1- https://www.thermofisher.com
2- https://experiments.springernature.com/